Область бдс желудка что это
Область бдс желудка что это
Лучший метод исследования большого дуоденального сосочка — интраоперационная холангиография. Если при интраоперационной холангиографии отмечается свободный пассаж рентгенеконтрастного вещества в даенадцатиперстную кишку и через узкий сегмент дистального отдела общего желчного протока, который может быть хорошо виден на рентгенограмме, инструментальное исследование фатерова сосочка выполнять не нужно. При наличии усиливающего экрана можно лучше оценить сфинктер Oddi и его функциональное состояние. Однако если необходимо производить холедохотомию для удаления конкрементов из общего желчного протока, обычно выполняют инструментальное исследование большого дуоденального сосочка, несмотря на его нормальное анатомическое строение и функцию, подтвержденные с помощью интраоперационной холангиографии.
Если при холангиографическом исследовании большого дуоденального сосочка выявлены анатомические и функциональные отклонения сфинктера Oddi и наличие ущемленных конкрементов, его инструментальная ревизия необходима.
Для исследования большого дуоденального сосочка безопаснее применять зонды, заостренные в форме оливы и сделанные из резины, пластика или шелка. Пластиковые или шелковые зонды являются полужесткими по сравнению с более мягкими резиновыми и более жесткими металлическими. Металлическими зондами можно пользоваться лишь в исключительных случаях, так как они могут травмировать общий желчный проток и большой дуоденальный сосочек. Если пользуются металлическими расширителями Bakes (несмотря на их название, так как они бьши изначально предназначены для расширения сосочка), их следует применять только только в качестве зондов, а не в качестве расширителей.
Принято считать, что дуоденальный сосочек не имеет стриктуры, если через него проходит расширитель Bakes диаметром 3 мм. Расширять сосочек совершенно не требуется, потому что, как правило, очень скоро он возвращается в прежнее состояние, а травма сосочка может вызвать его спазм, отек, гематому и даже разрыв. С другой стороны, попытки расширить сосочек силой могут привести к образованию опасных ложных ходов. Зонд, который легко прошел в двенадцатиперстную кишку, не следует без необходимости проводить несколько раз через фатеров сосочек для повторного подтверждения его проходимости. Этого вполне достаточно, для того чтобы его травмировать, что может вызвать спазм, отек и обтурацию.
В момент инструментального исследования фатерова сосочка необходимо установить, прошел ли исследующий инструмент через просвет сосочка или сосочек был вытолкнут этим инструментом. Для установления этих различий применяют следующие критерии оценки:
1. Если зонд прошел через просвет сосочка, он выпячивает стенку двенадцатиперстной кишки напротив него, производя впечатление, что почти перфорировал ее. Если используется металлический зонд, при этом появляется характерный блестящий металш-гческий оттенок, описанный Walzel в 1919 г. Признак Walzel не появляется, если зонд выталкивает сосочек вперед.
2. Если зонд прошел через сосочек, его конец свободно движется в просвете двенадцатиперстной кишки; этого не наблюдается, когда он выталкивает сосочек.
3. Если зонд проходит через сосочек, это обычно происходит на 4—5 см ниже уровня, на котором большой дуоденальный сосочек обнаружен.
4. При пальпации зонда устанавливают, что он не окружен тканью, а лежит свободно в просвете двенадцатиперстной кишки.
Выполняя ревизию дуоденального сосочка, необходимо помнить, что у некоторых пациентов просвет дистального общего желчного протока не соответствует просвету суженного сегмента (интрапариетальный сегмент). Просвет суженного сегмента имеет эксцентрическое или латеральное положение по отношению к сегменту общего желчного протока, который шире в диаметре и расположен над ним. В результате, когда зонд, легко проходя через дистальный отдел общего желчного протока, достигает суженного сегмента, расположенного латерально. он не входит прямо в просвет этого сегмента, а сталкивается с его стенкой. При этом хирург думает, что это сужение и является большим дуоенальным сосочком, что не совсем верно.
Эндоскопическая диагностика и лечение опухолей большого дуоденального сосочка
А. С. Балалыкин, Оноприев А. В., Муцуров Х. С., Катрич А. Н., Вербовский А. Н.
Москва, Краснодар
Актуальность
В настоящее время число воспалительных и опухолевых заболеваний поджелудочной железы, желчного протока и большого дуоденального сосочка (БДС), вызывающих непроходимость внепеченочных желчных протоков, продолжает увеличиваться и удельный вес рака БДС среди опухолей билиопанкреатодуоденальной зоны составляет 10,1–18,3 % (Русаков В. И. с соавт., 1986; Frosali D. et al., 1990).
Чрезвычайная злокачественность рака панкреато-биллиарной области и его поздняя диагностика приводят к тому, что хирургическое лечение больных сопровождается высоким операционным риском и невозможностью выполнения радикальных операций. Их частота составляет только 4–27 %, послеоперационная летальность достигает 8–22 %, а пятилетняя выживаемость — всего 4–6 % [М. В. Данилов соавт., 1995; А. А. Мовчун с соавт., 1994; В. А. Кубышкин с соавт., 2003].
Благодаря ранним клиническим проявлениям (механическая желтуха) опухоли БДС диагностируются на более ранней стадии, чем опухоли другой локализации. Существующие инструментальные методы исследования (эндоскопические, лучевые, лапароскопические) далеко не всегда позволяют сформулировать наиболее рациональную тактику и вид лечения, и главное, имеют существенные ограничения в оценке стадии болезни.
К 80-м годам прошлого столетия был разработан принципиально новый диагностический прибор — эхо-эндоскоп, соединивший в себе возможности гибковолоконной эндоскопии и ультразвукового исследования.
Отличительной особенностью и неоспоримым преимуществом метода перед другими является то, что ультразвуковой датчик под контролем зрения размещается в непосредственной близости от зоны исследования, что позволяет повысить разрешающую способность ультразвукового сканирования. Учитывая короткую дистанцию исследования, и доказанную корреляцию между получаемым ультразвуковым изображением и анатомическим строением стенки полых органов желудочно-кишечного тракта (ЖКТ), эндо-УЗИ позволяет произвести послойную структурную оценку БДС, окружающих его органов и тканей, сосудистых и протоковых образований в зоне исследования. Полученные данные позволяют установить диагноз и обосновать план лечения.
Материалы и методы исследования. Нами проанализированы результаты лечения 39 пациентов с подозрением на злокачественные новообразования диагностированные при обследовании 421 больных в 2004–2009 гг. в возрасте 35–77 лет.
Нами применен следующий инструментальный диагностический алгоритм: ТАУЗИ, фиброгастродуоденоскопия (ФГДС), эндо-УЗИ, эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ), фистулография, компьютерная томография (КТ) — по показаниям.
Несомненным преимуществом ТАУЗИ перед другими методами исследования является отсутствие противопоказаний и возможность использовать его в качестве экспресс-диагностического метода.
Перед ФГДС ставились следующие задачи: оценить проходимость верхнего отдела ЖКТ, выявить специфические изменения слизистой желудка и ДПК, характерные для сопутствующих заболеваний желудка и ДПК, определить доступность и состояние БДС и периампулярной области, оценить технические возможности проведения лечебных эндоскопических мероприятий на БДС.
Эндоскопическое ультразвуковое исследование.
Мы использовали видеоэндоскопический комплекс, EVIS EUS EXERA, «Olympus», Япония, включающий: видеоэндоскопический центр CV-160, осветитель CLV-160, ультразвуковой эндоскопический центр UM-60, радиальный ультразвуковой гастровидеоскоп GF-UM 160.
Подготовка больных к эндо-УЗИ панкреатобилиарной системы не отличается от таковой при обычной эндоскопии.
Проведению эндо-УЗИ обязательно должно предшествовать эндоскопическое или рентгенологическое исследование пищевода или желудка (для исключения стенозов, дивертикулов), поскольку введение эхоэндоскопа производится практически без визуального контроля.
Стандартные позиции проведения эндоскопического ультразвукового исследования различных органов были предложены M. Sivak (1982 г), и W. Strohm и M. Classen (1982) и утверждены Международной конференцией по эндоскопической эхографии (Стокгольм). В последствии методика была дополнена K. Inui et al. (2004).
Большой дуоденальный сосочек — осмотренный в поперечном сечении, представляется как дополнительное округлое (овальное) многослойное образование стенки нисходящего отдела ДПК. При идентификации структур БДС определяются поочередно мышечный слой ДПК (слой сниженной эхогенности), подслизистый слой ДПК (слой повышенной эхогенности), мышечный аппарат сфинктера (тонкий гипоэхогенный слой) и внутренний гиперэхогенный слой, соответствующий слизистому и подслизистому слою ампулы сосочка.
Для исследования БДС в продольном направлении необходимо смещение УЗ-датчика в проксимальном направлении, путем подтягивая эндоскопа. Основными ориентирами являются протоковые структуры; в этом случае ультразвуковая картина меняется индивидуально: соответственно анатомическим взаимоотношениям терминальных отделов желчного и панкреатического протоков, относительно друг друга и стенки ДПК.
Увеличение БДС в размерах более 1 см, выявление в просвете сосочка дополнительных образований, исходящих из его стенок, изменение эхографических характеристик многослойной структуры данного анатомического образования интерпретируется как патологическое изменение БДС.
Ультразвуковая семиотика заболеваний БДС. Эндоскопическими ультразвуковыми диагностическими критериями опухоли БДС являются: нарушение нормальной многослойной эхоструктуры БДС, солидное образование в проекции БДС, сниженная или смешанная эхо-генность образования, нечеткие контуры образования.
Опухоль может иметь экзофитную (в просвет ДПК) и эндофитную или инвертированную (в просвет дистальных отделов протоков) формы роста. На начальных стадиях роста и небольших размерах образования и при отсутствии инфильтративного роста надежных дифференциально-диагностических критериев карциномы и аденомы, не существует.
Эндоскопическими ультразвуковыми диагностическими критериями карциномы сосочка являются: распространение гипоэхогенных тканевых масс на мышечный слой стенки ДПК, в просвет холедоха и ГПП или на стенки протоков, в паренхиму поджелудочной железы, и/или обнаружение рядом с БДС лимфатических узлов подозрительных на их метастатическое поражение (Панцырев Ю. М. и соавт. 2002). Это- важные дифференциально-диагностические признаки, т. к. обнаружение хотя бы одного из них определяет тактику лечения и ставит под сомнение радикальность эндоскопической резекции опухоли. Недооценка указанных фактов приводит к неудовлетворительным результатам эндоскопических методов лечения.
Наиболее важными лимфатическими коллекторами, требующими детальной оценки для точного определения лимфогенного метастазирования опухоли БДС в процессе выполнения эндосонографии, являются лимфоузлы печеночно-двенадцатиперстной связки, задние поджелудочно-двенадцатиперстные лимфоузлы и верхнебрыжеечные лимфоузлы.
Так как опухоли БДС, которые инфильтрировали поджелудочную железу или периампулярную область, невозможно отличить от первичных панкреатических карцином, большинство авторов описывают их как «опухоли БДС» или «периампулярные раки». Так как оба типа в одинаковой степени склонны к метастазированию, нет необходимости в их дооперационной дифференцировке их локализации. Дооперационное определение стадии ампулярной карциномы базируется на основании Международной классификации по факторам TNM принятой европейской организацией «Union International Control Cancer».
Результаты
После комплексного применения диагностических методик у 36 из 421 обследованных пациента был установлен предварительный диагноз опухоли БДС, причем у 34 пациентов была заподозрена злокачественная природа процесса в стадии Т1 — у 7 (20,6 %), Т2 — у 16 (47 %), в стадии Т3 — у 11 (32,4 %) пациентов.
Нами была проанализирована диагностическая ценность инструментальных методов в диагностике опухолей БДС и установлено, что эндо-УЗИ имеет более высокую чувствительность, специфичность и диагностическую эффективность.
Показания к эндоскопическим методам лечения были выставлены у 7 пациентов. После применения комплекса диагностических методик, по макроскопической картине выявленные неоплазии были разделены на экзофитную и эндофитную (инвертированную) форму опухоли БДС. Размеры выявленных образований колебались в пределах от 8 до 32 мм. Морфологическая характеристика опухолей распределилась следующим образом: высокодифференцированная аденокарцинома, аденома с дисплазией III ст., аденома с дисплазией II ст.
Возможность выполнения эндоскопической эксцизии опухолей БДС (Балалыкин А. С. и соавт. 2008, Катрич А. Н. и соавт., 2008) обосновывалась данными эндо-УЗИ (тип роста образования, наличие измененных лимфатических узлов, состояние мышечного слоя стенки ДПК, терминальных отделов желчного и панкреатического протока). Всем пациентам был применен последовательный комплекс эндохирургических вмешательств, включавший атипичную «послойную» ЭПТ с помощью торцевого папиллотома, дополненная канюляционной ЭПТ у 6 больных, петельную электроэксцизию опухоли, электро — или аргоноплазменную деструкцию, а также вмешательства, направленные на обеспечение адекватного пассажа желчи и панкреатического сока (стент, НБД). Всем пациентам в послеоперационном периоде выполнялось желудочное и дуоденальное зондирование, проводился курс консервативной терапии. Контрольные обследования выполнялись в сроках от 3 до 6 месяцев.
Успех и безопасность эндоскопического вмешательства определяется правильным набрасыванием петли и рациональным сочетанием режимов резания и коагуляции, поэтому в зависимости от формы роста опухоли менялись технические аспекты выполнения данного этапа операции. В случае эндофитной формы роста опухоли после выполнения атипичной «послойной» ЭПТ, с помощью торцевого папиллотома выполнялись «полулунные» окаймляющие разрезы слизистой оболочки в пределах здоровых тканей, в 3 случаях дополненные введением с помощью инъектора, раствора в подслизистый слой, для создания «подушки» под тканью опухоли. С нашей точки зрения эти приемы обеспечивают:
1) адекватное набрасывание эндоскопической петли на опухоль;
2) снижают риск «сползания» петли;
3)резекцию «in block». С целью профилактики кровотечения и повышения абластичности операции выполнялась электро или аргоноплазменная деструкция зоны новообразования БДС. Обеспечение свободного пассажа желчи и панкреатического сока достигалось за счет выполнения билиопанкреатического стентирования.
Осложнениями оперативных вмешательств являлись: интраоперационное кровотечение, остановленное эндоскопически, микроперфорация ДПК, которая была излечена консервативно.
В одном случае, через 3 месяца после выполнения операции, при контрольном эндо-УЗИ, был выявлен продолжающийся рост опухоли. Пациенту была выполнена панкреатодуоденальная резекция.
Выводы
1. Методика эндоскопического ультразвукового исследования является наиболее эффективным методом диагностики заболеваний БДС, стадии злокачественного процесса и позволяет планировать объем и вид лечения больных. 2. Успех, радикальность и безопасность эндоскопической папиллэктомии определяется комплексностью эндоскопических методик и четким соблюдением этапности их выполнения. Включение в лечебный алгоритм стентирования протоков обеспечивает свободный пассаж желчи и панкреатического сока, и позволяет избежать послеоперационных осложнений.
Актуальность проблемы
Дуодено-гастральный рефлюкс (ДГР) — одна из самых распространенных патологий верхних отделов желудочно-кишечного тракта, по данным разных источников, данное нарушение занимает 50-90% от всех заболеваний ЖКТ. Более того, за последние годы прослеживается рост количества заболевших. У пациентов с дуоденогастральным рефлюксом нередко также диагностируется хронический гастрит, в том числе рефлюкс-гастрит типа С, щелочной гастрит, язвенная болезнь желудка, функциональная диспепсия, грыжа пищеводного отверстия диафрагмы и ГЭРБ, пищевод Барретта, дуоденостаз, дисфункция сфинктера Одди, постхолецистэктомический синдром, рак желудка и целый ряд других заболеваний.
Следует знать, что ДГР способен привести к тяжелому гастриту и эзофагиту, стать причиной метаплазии желудка и пищевода, а также плоскоклеточного рака пищевода, который развивается на фоне метаплазии; это подтверждено клиническими исследованиями.
Таким образом, в результате патологического рефлюкса дуоденального содержимого в желудок течение многих органических и функциональных патологий ЖКТ может осложняться. Поэтому огромное значение должно уделяться своевременной диагностике, правильной клинической интерпретации и адекватной медикаментозной терапии.
При неэффективности консервативной коррекции показано хирургическое вмешательство, целью которого является укрепление пилорического жома, а также снижение количества забрасываемой желчи в желудок.
Есть данные о том, что на фоне ДГР желудка часто развиваются симптомы поражения системы дыхания, появляется синдром боли в грудной клетке, который не связан с коронарной патологией. Кроме того, у некоторых пациентов дуоденогастральный рефлюкс может вызвать рецидивирующий катаральный фарингит и пароксизмальный ларингоспазм. Однако у трети больных диагностируется «чистый» дуодено-гастральный рефлюкс, в этом случае можно говорить об изолированном диагнозе.
Причины дуодено-гастрального рефлюкса
Патогенетический механизм развития осложнений при ДГР
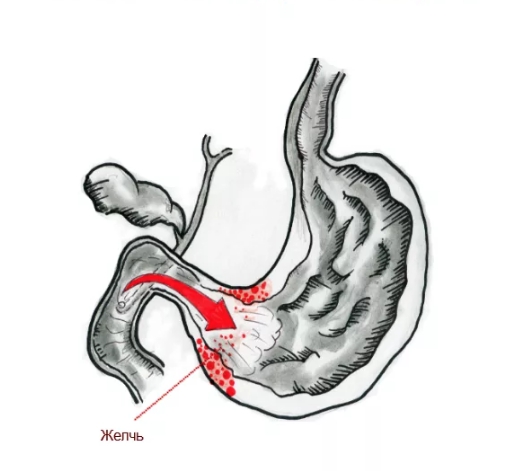
Желчь в составе рефлюксата при патологическом дуодено-гастральном рефлюксе ретроградно поступает из ДПК в органы, расположенные выше — желудок с пищеводом. Желчные кислоты, трипсин, лизолецитин — составляющие дуоденального содержимого — повреждают слизистую оболочку. Наиболее агрессивным действием при забросе дуоденального содержимого обладают желчные кислоты. Сегодня уже доказано, что при кислом рН среды лизолецитин и конъюгированные желчные кислоты (прежде всего тауриновые конъюгаты) сильнее повреждают слизистую желудка и пищевода, что определяет синергизм этих компонентов с соляной кислотой в развитии эзофагита и гастрита.
Неконъюгированные желчные кислоты и трипсин обладают более токсичным действием при слабощелочном и нейтральном рН, повреждающий эффект при дуодено-гастральном рефлюксе увеличивается при медикаментозном подавлении кислого рефлюкса. Их токсичность большей частью вызвана ионизированной формой, благодаря чему кислоты легко проникают через слизистую пищевода и желудка. Исходя из этого вполне объяснимо отсутствие адекватного ответа у 15-20% пациентов при монотерапии антисекреторными препаратами, если не будет учтен имеющийся дуодено-гастральный рефлюкс.
В результате действия на слизистую желудка желчных кислот, содержащихся в желчи, в течение длительного времени возникают изменения поверхностного эпителия желудка дистрофического и некробиотического характера, что ведет к развитию рефлюксгастрита — гастрита С. При имеющейся инфекции Нelicobacter pylori повреждающее действие рефлюксата на слизистую желудка возрастает. При наличии ДГР происходит заброс агрессивного содержимого в вышележащие отделы, что становится причиной нарушений в работе пищеварительной системы, воздействию подвергается мембранное и полостное пищеварение, возможность всасывания пищевых ингредиентов с микроэлементами и витаминами, изменяется водный баланс.
Признаком негативного воздействия ДГР являются признаки атрофии, метаплазии и дисплазии, это представляет опасность из-за риска развития рака желудка или пищевода. Кроме того, желчь в сочетании с панкреатическим соком из-за своей агрессивности разрушающе действует на слизистый барьер в желудке, при этом обратная диффузия водородных ионов усиливается. В результате этих процессов возникают эрозивные и язвенные поражения слизистой оболочки желудка.
Клинические проявления и диагностика дуодено-гастрального рефлюкса
Для ДГР характерно преобладание диспептических проявлений, пациента беспокоит отрыжка кислым содержимым или воздухом, изжога, тошнота, возможна рвота желчью, также появляется горечь во рту, которая не исчезает и даже усиливается при приеме ингибиторов протонной помпы.
Периодические боли в животе чаще схваткообразного характера, они могут возникать вследствие стресса или физической нагрузки.
Чаще дуоденогастральный рефлюкс сочетается с другими заболеваниями ЖКТ, в первую очередь с язвой желудка и ДПК, ГПОД, хроническим холециститом, панкреатитом и др. Соответственно, это отражается на симптоматике рефлюкса, существенно ее маскируя. В «чистом» виде ДГР появляется не так часто.
Дуодено-гастральный рефлюкс, в отличие от «классического» — желудочно-пищеводного рефлюкса кислой природы с изжогой, дисфагией и регургитацией — сопровождается не столь яркими клиническими проявлениями, но чаще проявляются признаки диспепсии. Кроме того, больных беспокоит боль в эпигастральной области, которая становится сильнее после приема пищи.
Диагностика основывается на результатах инструментальных методов обследования.
Лечение дуодено-гастрального рефлюкса
Консервативное лечение ДГР желудка отличается сложностью, целью терапии является нейтрализация агрессивного воздействия дуоденального содержимого на слизистую желудка и пищевода. Также в задачи лечения входит нормализация пропульсивной способности пищеварительного тракта. Назначения включают прокинетики, антациды, сорбенты, препараты урсодезоксихолевой кислоты (УДХК). При желчном рефлюксе терапия сочетается с базисным лечением основного заболевания. При этом огромное значение уделяется соблюдению диеты.
Медикаменты, используемые для устранения ДГР и восстановления моторики ЖКТ:
Следует учесть, что эритромицин в качестве прокинетика не рекомендован из-за побочных эффектов, цизаприд — не показан в клинической практике из-за вероятности нарушения сердечной проводимости, тегасерод — увеличивает вероятность инфаркта миокарда.
Фармакологическое действие домперидона (D2 антагонист) и метоклопрамида (5 НТ4 агонист и D2 антагонист) связано с блокадой рецепторов дофамина, антагонисты которых вызывают повышение тонуса нижнего сфинктера пищевода, увеличивают сократительную функцию желудка, а также препятствуют релаксации. Кроме того, благодаря антагонистам дофаминовых рецепторов улучшаются эвакуаторная способность желудка и антродуоденальная координация, что способствует устранению дуодено-гастрального рефлюкса.
Важно учесть, что клинические проявления рефлюкса с использованием медикаментозных препаратов уменьшаются, однако носят симптоматический характер. Добиться хороших результатов можно только при функциональных нарушениях, которые привели к ДГР. В остальных случаях консервативная терапия должна сочетаться с хирургическим лечением, способным устранить причину рефлюкса и укрепить пилорический клапан.
Хирургическое лечение дуодено-гастрального рефлюкса
При неэффективности консервативной терапии рекомендовано оперативное лечение, операция при этом проводится в нескольких направлениях:
При всех вышеперечисленных методиках используется лапароскопический доступ — через несколько (3-4) проколов на брюшной стенке.
Техника лапароскопической пилоропликации для уменьшения дуодено-гастрального рефлюкса
Прежде всего проводится ревизия пилородуодальной зоны, и оценивается выраженность спаечного процесса в зоне луковицы ДПК и привратника. Затем необходимо осмотреть связку Трейца, в случае необходимости она пересекается, тем самым улучшается прохождение пищи по двенадцатиперстной кишке. После ее мобилизации по Кохеру, что сделает ее более подвижной и снизит напряжение, накладываются швы в области привратника, что служит для профилактики несостоятельности.
Для пилоропликации поочередно накладываются серозно-мышечные швы симметрично к осе привратника, благодаря подобной методике передняя стенка луковицы ДПК сдвигается в проксимальном направлении, передняя полуокружность привратника погружается в просвет луковицы ДПК. Обычно четырех швов достаточно. Созданный антирефлюксный механизм способен препятствовать ДГР, не нарушая при этом эвакуации из желудка.
При необходимости проводится коррекция ГПОД или выполняется вмешательство на билиарном тракте. Следует помнить, что при лапароскопии возможно выполнение нескольких симультанных операций при наличии патологий в брюшной полости, малого таза или в забрюшинном пространстве, требующих оперативного лечения (киста почки, яичника, нефроптоз, миома и др.).
К настоящему времени нашими специалистами проведено более чем 600 оперативных вмешательств по поводу ГПОД и рефлюкс-эзофагита, а также связанных с хроническим нарушением дуоденальной проходимости. Накопленный опыт обобщен в 4-х монографиях: «Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии», «Грыжи пищеводного отверстия диафрагмы», «Ручной шов в эндоскопической хирургии» и «Технология дозированного лигирующего– электротермического воздействия на этапах лапароскопий». Кроме того, информация опубликована в многочисленных научных публикациях в разных профессиональных рецензируемых научных изданиях — российских и зарубежных.
После вмешательства на коже живота останется лишь несколько разрезов, длина которых не превышает 10 мм. Уже в день операции пациенты могут вставать, разрешается пить, на следующий день можно принимать теплую пищу в жидком виде. Клинику можно покинуть на 1-3 день — возможность выписки зависит от тяжести состояния. Но уже спустя 2-3 недели человек может вернуться к привычному образу жизни. Соблюдение строгой диеты необходимо в ближайшие два месяца, более мягкая разрешена через полгода после вмешательства. В дальнейшем человек, перенесший операцию, может обходится без медикаментов и не нуждается в строгом соблюдении диеты.
По желанию наши пациенты могут перед оперативным лечением пройти полное обследование, по результатам которого будет подобрана оптимальная тактика лечения и метод хирургического вмешательства.
На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное — свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие. Каждый день я по нескольку часов отвечаю на ваши письма. Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы. Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии.
Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи. Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами.
В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.